Hvorfor evolusjonen fant opp et enzym som spiser opp vitamin B3
Matematisk modellering og systembiologi forklarer den evolusjonære overgangen fra en fire-trinns til en to-trinns vei for syntese av NAD fra vitamin B3.

Hovedinnhold
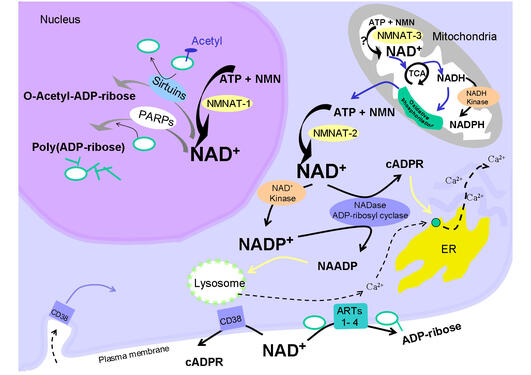
Vann, ATP og DNA blir ofte nevnt av mange forskere når man spør om livets viktigste molekyl. Hvis du spør medlemmer av forskningsgruppen til Mathias Ziegler ved Institutt for biomedisin, vil de helt sikkert legge nikotinamid adenin dinukleotid (NAD) til den listen.
NAD (PubChem ID 5892) er utvilsomt en kjendis i den biokjemiske verden. Den er sammenlignbar med et oppladbart batteri som transporterer elektroner når kjemisk energi lagret i næringsstoffene blir omdannet til ATP, den universelle energivalutaen. Liv er ikke mulig uten NAD, og derfor finnes dette molekylet i alle organismer, fra bakterier til mennesker. Ettersom organismene ble mer komplekse i løpet av evolusjonen, har det oppstått nye prosesser som er avhengige av NAD, for eksempel DNA-reparasjon, cellesyklus og genregulering, som er viktige for menneskers helse og sykdom. Disse nye funksjonene til NAD gjør at NAD blir fortløpende brukt opp. Det krever derfor tilsvarende kontinuerlig biosyntese av NAD, som lages av vitamin B3.
Et konsortium av laboratorier fra Norge, Tyskland og Storbritannia, ledet av Ines Heiland fra Institutt for arktisk og marin biologi ved Arctic University of Norway i Tromsø, ville vite mer om dette kretsløpet.
Tre hovedobservasjoner…
Forskerne brukte en beregningsorientert metode for å følge utviklingen av stoffskiftet til vitamin B3 gjennom evolusjonen, og gjorde tre spennende observasjoner:
- NAD-syntese foregår i en biokjemisk prosess som bruker fire trinn i lavere organismer, mens høyere organismer bruker en to-trinns prosess. Forskerne fant ut at skiftet fra fire til to trinn skjedde samtidig som organismene fant opp et nytt enzym som er tilsynelatende paradoksalt. Det enzymet er kalt nikotinamid N-methyltransferase (NNMT).
Ved første blikk oppfører NNMT seg som en slemming i stoffskiftet: Det forhindrer praktisk talt at vitamin B3 kan brukes som NAD-forløper. Hvorfor skapte naturen et enzym som fjerner noe som er helt nødvendig for cellen? - Mens forskerne analyserte NAD-stoffskifte gjennom hele livets tre, fant de ut at det “paradoksale” enzymet NNMT ble til da høyere livsformer utviklet nye mekanismer som bruker NAD.
- Forskerne oppdaget at evolusjonen hadde dannet en ny form av enzymet NamPT (eller nikotinamidfosforibosyltransferase), omtrent ved samme tid som det paradoksale NNMT hadde dukket opp. Denne nye NamPT-formen inneholder en håndfull flere aminosyrer enn før. Dette funnet vakte forskernes oppmerksomhet, siden NamPT er involvert i terapeutiske konsepter på grunn av sin sentrale rolle i omforming av vitamin B3 til NAD.
... og en overraskende enkel forklaring
Forskerne i Tromsø utviklet matematiske modeller for å analysere NAD-avhengige stoffskifteveier, og for å simulere enzymer involvert i dannelse og forbruk av NAD. Ved hjelp av disse modellene kunne de gi en ganske enkel forklaring på fremveksten av enzymet NNMT. Organismene utviklet nye stoffskifteveier som forbruker NAD og produserer nikotinamid. Sistnevnte hoper seg opp og hemmer akkurat disse veiene. Når NNMT er til stede, så vil det forhindre at nikotinamid hoper seg opp, og dermed muliggjøre en høy omsetning av NAD. Så langt er alt bra. Men hvorfor har også enzymet NamPT tilpasset seg? Hvorfor er det moderne NamPT utstyrt med ti ekstra aminosyrer?
For å svare på dette spørsmålet ba forskerne fra Tromsø om hjelp fra laboratoriet til Mathias Ziegler ved Institutt for biomedisin.
Fra tørrlab til våtlab ved Institutt for biomedisin ...
Dorothée Houry og Marc Niere hadde som mål å belyse rollen til de ti nye aminosyrene i det moderne NamPT ved å bruke det menneskelige enzymet som eksperimentell modell. De ville vite hvordan de viktigste egenskapene til det menneskelige NamPT endres når enzymet blir konvertert tilbake til den gamle versjonen. For dette formålet tok de ut de ti ekstra aminosyrene av det menneskelige enzymet og målte aktiviteten. De så at det modifiserte enzymet var langt mindre effektivt enn det opprinnelige enzymet når det gjaldt å konvertere nikotinamid. Med andre ord: det modifiserte menneskelige NamPT-enzymet etterlignet den versjonen som finnes i bakterier. Disse eksperimentelle dataene stemte helt overens med den fylogenetiske modellen utviklet i Tromsø. Enzymet NamPT ble optimalisert, slik at det kunne gjennomføre den beste NAD-syntesen i en verden der mange nye signalomformingsveier begynte å bruke opp NAD.
... og videre til pasientsengen?
Selv om disse funnene er fascinerende for evolusjonsbiologer og biokjemikere, har de også potensielle medisinske implikasjoner. Det finnes for eksempel terapeutiske konsepter som manipulerer aktiviteten til NamPT, og det er påvist at enzymet NNMT hoper seg opp i noen krefttyper. De nye forskningsfunn burde derfor tas i betraktning når man utvikler terapier og legemidler.
Denne forskningen er publisert i Proceedings of the National Academy of Sciences of U.S.A. (PNAS) i august 2019. https://www.pnas.org/content/116/32/15957